新着情報
Informations

雑誌会
2025.04.08
フラーレン誘導体を光フローケミストリーで
この『雑誌会』は、化学系の雑誌を中心に独断と偏見で研究例を選び、不定期でご紹介するコーナーです。
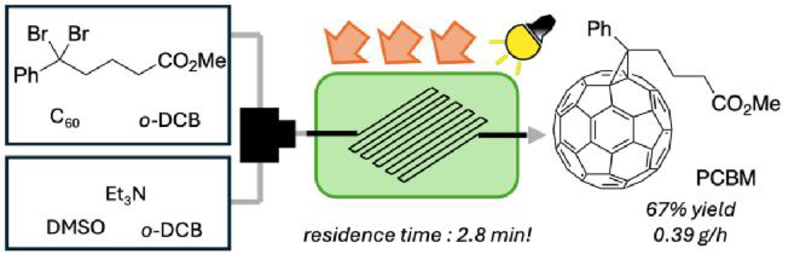
サッカーボール型の炭素物質であるフラーレンC60やC70の置換基導入をフォトフローで試みたお話です。
PCBM synthesis using photoflow strategy
Shuhei Sumino1,* , Yuya Tanaka2, Michihisa Murata2 , Fukashi Matsumoto1, Toshiyuki Iwai1,Takatoshi Ito1
Chemistry Letters, 2024, Vol. 53, No. 12
(本文)
https://academic.oup.com/chemlett/article/53/12/upae219/7906724
(補足情報)
https://oup.silverchair-cdn.com/oup/backfile/Content_public/Journal/chemlett/53/12/10.1093_chemle_upae219/15/upae219_supplementary_data.pdf?Expires=1740531815&Signature=GPuZmwUjr-uZZkJ4J5ZamOVATmXAbXnXM~7NxFh0PgvjjLO3wGlYDI0zd0oGf8n1XQSyYUtw24r7Vwv9KEM-qxD0mSs3l6rO-hWwL5SeQUghtL75sZNXxx~esWvNf5IeL0aBY66FMaKrHEgDmO-IJEeId6~g~rntrDMOSy8ZBjGzhFTqJ4Qi~du9tzLXYSSvzycAnSISMuZY52HI7YSXmR9uEjmOtLfrf8rAh5PVEhpAy96XRLfKA4DBsPzZ35cY4MPIIF~DAjw6bmrubIXW6MdwPPAn~mLelrYTJi-Lbab4NB9aUgcMAasbblI9l-XNxu79wCZ0izkvgiCZma~ZCw__&Key-Pair-Id=APKAIE5G5CRDK6RD3PGA
まず、フラーレンについてです。
『フラーレンは炭素原子が球状の構造を成している化合物の総称で,ダイヤモンドや黒鉛,カーボンナノチューブと同様に炭素の同素体です。フラーレンは,分子性の単一の化学種として単離することが可能な炭素化合物で,C60,C70,C84などが知られています。』『フラーレンの最も特筆すべき点は,フラーレンが優れた電子受容体であるということにあります。フラーレンはn型半導体の性質を持っており,電子をキャリアとする有機エレクトロニクス材料として幅広く研究されています。ルビジウムやセシウムをドープしたフラーレンは電子をキャリアとする超伝導体となり,30 K以上で超伝導転移を起こすことが報告されています。』とあります。
(フラーレン)
https://www.tcichemicals.com/JP/ja/c/12961
しかしながら、C60やC70には問題点もあるようです。
『C60, C70などのフラーレンやカーボンナノチューブなどの炭素ナノ材料は、電子機能材料として有望な材料ですが、そのままでは汎用有機溶剤に対する溶解性に乏しく薄膜などへの成型加工が困難なため、可溶化を目指した官能基の化学修飾を行なっています。 これまでに有機薄膜太陽電池用アクセプター材料として一連のメタノフラーレン誘導体を開発してきており、また、光反応性の置換基を有する化合物とフラーレンを光化学反応させることで、より効率よく選択的にフラーレンの化学修飾反応を起こす反応系の構築を目指しています。』とあります。
(炭素ナノ材料の可溶化を指向した新規化学修飾反応の開発)
https://orist.jp/kenkyu-bu/yuki-zairyo/fms/
そして、『マイクロリアクターは数μmから数百μm程度の微細流路を持つ微小な反応容器ではありますが、フロー方式(連続送液)で使用するため大量製造にも適用可能であり、研究室におさまるような小型の反応装置を用い年間数千トン規模での製造も見込まれています。』『本研究室では、マイクロリアクターによるフロー・マイクロ合成の手法を用いて、有機金属試薬を利用した合成反応開発や、逐次反応制御を目的とした有機薄膜太陽電池材料合成の選択性の改善について取り組んでいます。』とあり、今回の研究例も『マイクロリアクターによるフロー・マイクロ合成の手法を用いてC60, C70などのフラーレンの可溶化を目指した官能基の化学修飾』を試みたようです。
(フローマイクロリアクターを利用した高選択的合成法の開発)
https://orist.jp/kenkyu-bu/yuki-zairyo/fms/
図1が目的物です。
Scheme 1 のaとbに過去の研究例が描かれています。
Schem 1のaはオーソドックスなバッチ方です。
a-a、a-bは収率が低く、a-cは収率が93%と非常に高いものの、実現させるには不活性ガスのコントロールが超難しいみたいです。
Scheme 1のbはフロー方式で、ヒドラゾンをつかった方法のようです。b-aは加熱するだけ、b-bは加熱+光のようです。いずれも収率が30%台とあまり良くなかったようです。
そこで、今回の研究例では化合物1とトリエチルアミンを用いてC60の修飾をフォトフローで試みたようです。
化合物1の特徴として、臭素が2つ同じ炭素原子と結合しているところのようです。
これについては、参考文献6の図4に今回の研究例の図1にあるPC61BMとPC71BMの合成例が示してあり、この参考文献6の研究例をお手本としたようです。
(参考文献6、Manganese powder promoted highly efficient and selective synthesis of fullerene monoand biscycloadducts at room temperature)
https://www.nature.com/articles/srep13920
図2に装置系の図が描かれています。送液はシリンジポンプとあります。イメージ的には下記の図1ではないか?と思われます。
(有機化学を高速化する)
https://www2.sci.hokudai.ac.jp/dept/chem/change/nagaki-aiichiro
シリンジポンプはシリンダーの中の液を全て出し切るとそこで終了です。今回の研究例では試作実験なので、送液量は有限で良かったのだろうと思われますが、将来的には連続ポンプの使用に移行するものと考えられます。
図2でシリンジAにはC60と化合物1のo-ジクロロベンゼン(o-DCB、 https://labchem-wako.fujifilm.com/jp/product/detail/W01W0104-0778.html )溶液、シリンジBにはトリエチルアミンのDMSO/ o-ジクロロベンゼン混合溶媒による溶液が準備されたようです。
送液して、T-unionで二つの溶液は混合して反応容器へ流すようです。反応容器はパーフルオロアルコキシアルカン(PFA)製で温度も設定できるようです。今回の研究例では光反応を行うため、透明のPFAを用いたようです。温度は0~25℃はメタノールバスで、40~80℃はウォーターバスで冷却あるいは加熱したようです。
PFAとPTFAの違いについては、
(PTFEとPFAの違いと適切な用途別選択法)
https://yukosyokai.co.jp/column/2281/
結果です。
表1には化合物1の仕込み量、あるいはトリエチルアミンの仕込み量、そして滞留時間を変えた場合の影響について調べた結果が出ています。室温で実施したようです。
このような検討の場合、動かす変数は1つにしておくことが鉄則ですが、表1を見ると、二つ以上変わっている場合があり、話がややこしくなっています。
この点について、著者に直接尋ねてみると、快く返答が来ました。
『拙稿をご覧いただきありがとうございます。
ご質問いただいた点につきまして、下記に回答させていただきます。
※表1について
ご指摘のように、条件検討の場合は変数を2つ以上変化させないことが基本と考えております。表1だけをご覧になられた場合では、試薬の等量と反応時間のどちらもを変化させているように見えてしまうのですが、Supplementary data P7,8のFigure S5,6をご覧いただけますと、各等量、反応時間における収率の変化を記載しております。紙面の関係上、表1にはPCBMの収率が極大となる反応時間を記載しております。』
実は完全にSupplementary dataの存在を見落としておりました。確かにSupplementary dataを見ると、納得の行く内容となっております。
また、装置構成も補足情報の図S3を見れば良くわかります。
なお、補足情報の図S5や図S6を見ますと、滞留時間が長くなると、収率が下がることもあるようです。ただ、その場合、副生成物であるbis-PCBMが生成しているからのようです。図S5や図S6ではPCBMとbis-PCBMを分けてグラフが描かれていますが、誘導体を生成したということでまとめてしまい、(PCBM+bis-PCBM)とすれば、辻褄が合うような気がします。
しからば、bis-PCBMは悪者が否か?になります。もちろん、目的物はPCBMですが、置換基が増えれば、溶剤への溶解性も上がるでしょうし、必ずしも悪者にする必要はないかもしれません。もっとも、光化学特性においては、置換基は一つだけの方が良いかもしれず、このあたりについて識者の方々からご教示いただければと思います。
続いて、図3では光を14Wに固定して、反応容器の温度を変えた結果です。温度が高いほど短時間で目的物が生成して効率が上がる傾向は見られました。ただ、温度が70℃から80℃に10℃上げただけで、滞留時間は大きく伸び、効率がぐっと悪くなりました。
これはなぜでしょうか?
そこで著者に尋ねたところ、『確認することが難しいため、あくまでも推測になりますが、熱的に不安定な化合物1の分解を想定しております。』という返答でした。ただ、その後に思ったのですが、原料である化合物1が分解していたのであれば、収率の最高点も大きく下がってしまうのではないか?化合物1は必ずしも分解していたわけではないのでは?とも思いましたが、いかがでしょうか?
補足情報の図S7にLEDの光エネルギーが14 W、設定温度が 40 °C、ポンプの流量がシリンジAとBのどちらも157 μL/min、反応容器の大きさが滞留時間が5.0 min、100分間連続運転した場合の結果が示されています。概ね安定し、目的物が1時間当たり83mg得られたようです。
最後にLEDのエネルギーを14Wから58Wに引き上げ、温度も40℃から70℃に引き上げた一方で、滞留時間を5分から2.75分まで短縮させたところ、目的物が1時間あたり、83.1mgから388.8 mgまで上昇したようです。
更に、図4に見られますように、長時間の運転でも安定していたようです。
所感です。
フローケミストリーですが、その手の本を見ると、過去例として、非常にマニアックな合成例が出ていて、馴染みも得られず、非現実的な話と思ってしまいます。確かに偉~いセンセイ方にとっては、これまで不可能だった合成ができるようになれば、新規性あり、インパクトファクターの高い雑誌にも掲載され、ホクホク顔になれると思います。ただ、その結果、フローケミストリーの普及を著しく遅らせる要因だったように思います。今回の研究例では、手法や得られた化合物の利用方法なども現実的であり、いわゆる『役に立つ研究』ではないか?と思います。
サッカーボール型の炭素物質であるフラーレンC60やC70の置換基導入をフォトフローで試みたお話です。
PCBM synthesis using photoflow strategy
Shuhei Sumino1,* , Yuya Tanaka2, Michihisa Murata2 , Fukashi Matsumoto1, Toshiyuki Iwai1,Takatoshi Ito1
Chemistry Letters, 2024, Vol. 53, No. 12
(本文)
https://academic.oup.com/chemlett/article/53/12/upae219/7906724
(補足情報)
https://oup.silverchair-cdn.com/oup/backfile/Content_public/Journal/chemlett/53/12/10.1093_chemle_upae219/15/upae219_supplementary_data.pdf?Expires=1740531815&Signature=GPuZmwUjr-uZZkJ4J5ZamOVATmXAbXnXM~7NxFh0PgvjjLO3wGlYDI0zd0oGf8n1XQSyYUtw24r7Vwv9KEM-qxD0mSs3l6rO-hWwL5SeQUghtL75sZNXxx~esWvNf5IeL0aBY66FMaKrHEgDmO-IJEeId6~g~rntrDMOSy8ZBjGzhFTqJ4Qi~du9tzLXYSSvzycAnSISMuZY52HI7YSXmR9uEjmOtLfrf8rAh5PVEhpAy96XRLfKA4DBsPzZ35cY4MPIIF~DAjw6bmrubIXW6MdwPPAn~mLelrYTJi-Lbab4NB9aUgcMAasbblI9l-XNxu79wCZ0izkvgiCZma~ZCw__&Key-Pair-Id=APKAIE5G5CRDK6RD3PGA
まず、フラーレンについてです。
『フラーレンは炭素原子が球状の構造を成している化合物の総称で,ダイヤモンドや黒鉛,カーボンナノチューブと同様に炭素の同素体です。フラーレンは,分子性の単一の化学種として単離することが可能な炭素化合物で,C60,C70,C84などが知られています。』『フラーレンの最も特筆すべき点は,フラーレンが優れた電子受容体であるということにあります。フラーレンはn型半導体の性質を持っており,電子をキャリアとする有機エレクトロニクス材料として幅広く研究されています。ルビジウムやセシウムをドープしたフラーレンは電子をキャリアとする超伝導体となり,30 K以上で超伝導転移を起こすことが報告されています。』とあります。
(フラーレン)
https://www.tcichemicals.com/JP/ja/c/12961
しかしながら、C60やC70には問題点もあるようです。
『C60, C70などのフラーレンやカーボンナノチューブなどの炭素ナノ材料は、電子機能材料として有望な材料ですが、そのままでは汎用有機溶剤に対する溶解性に乏しく薄膜などへの成型加工が困難なため、可溶化を目指した官能基の化学修飾を行なっています。 これまでに有機薄膜太陽電池用アクセプター材料として一連のメタノフラーレン誘導体を開発してきており、また、光反応性の置換基を有する化合物とフラーレンを光化学反応させることで、より効率よく選択的にフラーレンの化学修飾反応を起こす反応系の構築を目指しています。』とあります。
(炭素ナノ材料の可溶化を指向した新規化学修飾反応の開発)
https://orist.jp/kenkyu-bu/yuki-zairyo/fms/
そして、『マイクロリアクターは数μmから数百μm程度の微細流路を持つ微小な反応容器ではありますが、フロー方式(連続送液)で使用するため大量製造にも適用可能であり、研究室におさまるような小型の反応装置を用い年間数千トン規模での製造も見込まれています。』『本研究室では、マイクロリアクターによるフロー・マイクロ合成の手法を用いて、有機金属試薬を利用した合成反応開発や、逐次反応制御を目的とした有機薄膜太陽電池材料合成の選択性の改善について取り組んでいます。』とあり、今回の研究例も『マイクロリアクターによるフロー・マイクロ合成の手法を用いてC60, C70などのフラーレンの可溶化を目指した官能基の化学修飾』を試みたようです。
(フローマイクロリアクターを利用した高選択的合成法の開発)
https://orist.jp/kenkyu-bu/yuki-zairyo/fms/
図1が目的物です。
Scheme 1 のaとbに過去の研究例が描かれています。
Schem 1のaはオーソドックスなバッチ方です。
a-a、a-bは収率が低く、a-cは収率が93%と非常に高いものの、実現させるには不活性ガスのコントロールが超難しいみたいです。
Scheme 1のbはフロー方式で、ヒドラゾンをつかった方法のようです。b-aは加熱するだけ、b-bは加熱+光のようです。いずれも収率が30%台とあまり良くなかったようです。
そこで、今回の研究例では化合物1とトリエチルアミンを用いてC60の修飾をフォトフローで試みたようです。
化合物1の特徴として、臭素が2つ同じ炭素原子と結合しているところのようです。
これについては、参考文献6の図4に今回の研究例の図1にあるPC61BMとPC71BMの合成例が示してあり、この参考文献6の研究例をお手本としたようです。
(参考文献6、Manganese powder promoted highly efficient and selective synthesis of fullerene monoand biscycloadducts at room temperature)
https://www.nature.com/articles/srep13920
図2に装置系の図が描かれています。送液はシリンジポンプとあります。イメージ的には下記の図1ではないか?と思われます。
(有機化学を高速化する)
https://www2.sci.hokudai.ac.jp/dept/chem/change/nagaki-aiichiro
シリンジポンプはシリンダーの中の液を全て出し切るとそこで終了です。今回の研究例では試作実験なので、送液量は有限で良かったのだろうと思われますが、将来的には連続ポンプの使用に移行するものと考えられます。
図2でシリンジAにはC60と化合物1のo-ジクロロベンゼン(o-DCB、 https://labchem-wako.fujifilm.com/jp/product/detail/W01W0104-0778.html )溶液、シリンジBにはトリエチルアミンのDMSO/ o-ジクロロベンゼン混合溶媒による溶液が準備されたようです。
送液して、T-unionで二つの溶液は混合して反応容器へ流すようです。反応容器はパーフルオロアルコキシアルカン(PFA)製で温度も設定できるようです。今回の研究例では光反応を行うため、透明のPFAを用いたようです。温度は0~25℃はメタノールバスで、40~80℃はウォーターバスで冷却あるいは加熱したようです。
PFAとPTFAの違いについては、
(PTFEとPFAの違いと適切な用途別選択法)
https://yukosyokai.co.jp/column/2281/
結果です。
表1には化合物1の仕込み量、あるいはトリエチルアミンの仕込み量、そして滞留時間を変えた場合の影響について調べた結果が出ています。室温で実施したようです。
このような検討の場合、動かす変数は1つにしておくことが鉄則ですが、表1を見ると、二つ以上変わっている場合があり、話がややこしくなっています。
この点について、著者に直接尋ねてみると、快く返答が来ました。
『拙稿をご覧いただきありがとうございます。
ご質問いただいた点につきまして、下記に回答させていただきます。
※表1について
ご指摘のように、条件検討の場合は変数を2つ以上変化させないことが基本と考えております。表1だけをご覧になられた場合では、試薬の等量と反応時間のどちらもを変化させているように見えてしまうのですが、Supplementary data P7,8のFigure S5,6をご覧いただけますと、各等量、反応時間における収率の変化を記載しております。紙面の関係上、表1にはPCBMの収率が極大となる反応時間を記載しております。』
実は完全にSupplementary dataの存在を見落としておりました。確かにSupplementary dataを見ると、納得の行く内容となっております。
また、装置構成も補足情報の図S3を見れば良くわかります。
なお、補足情報の図S5や図S6を見ますと、滞留時間が長くなると、収率が下がることもあるようです。ただ、その場合、副生成物であるbis-PCBMが生成しているからのようです。図S5や図S6ではPCBMとbis-PCBMを分けてグラフが描かれていますが、誘導体を生成したということでまとめてしまい、(PCBM+bis-PCBM)とすれば、辻褄が合うような気がします。
しからば、bis-PCBMは悪者が否か?になります。もちろん、目的物はPCBMですが、置換基が増えれば、溶剤への溶解性も上がるでしょうし、必ずしも悪者にする必要はないかもしれません。もっとも、光化学特性においては、置換基は一つだけの方が良いかもしれず、このあたりについて識者の方々からご教示いただければと思います。
続いて、図3では光を14Wに固定して、反応容器の温度を変えた結果です。温度が高いほど短時間で目的物が生成して効率が上がる傾向は見られました。ただ、温度が70℃から80℃に10℃上げただけで、滞留時間は大きく伸び、効率がぐっと悪くなりました。
これはなぜでしょうか?
そこで著者に尋ねたところ、『確認することが難しいため、あくまでも推測になりますが、熱的に不安定な化合物1の分解を想定しております。』という返答でした。ただ、その後に思ったのですが、原料である化合物1が分解していたのであれば、収率の最高点も大きく下がってしまうのではないか?化合物1は必ずしも分解していたわけではないのでは?とも思いましたが、いかがでしょうか?
補足情報の図S7にLEDの光エネルギーが14 W、設定温度が 40 °C、ポンプの流量がシリンジAとBのどちらも157 μL/min、反応容器の大きさが滞留時間が5.0 min、100分間連続運転した場合の結果が示されています。概ね安定し、目的物が1時間当たり83mg得られたようです。
最後にLEDのエネルギーを14Wから58Wに引き上げ、温度も40℃から70℃に引き上げた一方で、滞留時間を5分から2.75分まで短縮させたところ、目的物が1時間あたり、83.1mgから388.8 mgまで上昇したようです。
更に、図4に見られますように、長時間の運転でも安定していたようです。
所感です。
フローケミストリーですが、その手の本を見ると、過去例として、非常にマニアックな合成例が出ていて、馴染みも得られず、非現実的な話と思ってしまいます。確かに偉~いセンセイ方にとっては、これまで不可能だった合成ができるようになれば、新規性あり、インパクトファクターの高い雑誌にも掲載され、ホクホク顔になれると思います。ただ、その結果、フローケミストリーの普及を著しく遅らせる要因だったように思います。今回の研究例では、手法や得られた化合物の利用方法なども現実的であり、いわゆる『役に立つ研究』ではないか?と思います。
pdfはこちら
一覧に戻る







